Améliorer la reproductibilité des manipulations en culture cellulaire
Sources de variation durant la manipulation
Le stress
Les paramètres de culture cellulaire font l’objet d’un suivi régulier afin d'obtenir des cellules reproductibles et viables, mais les variations dans les techniques de manipulation restent souvent ignorées. Une analyse des possibles variations dans des applications de dépistage du cancer a révélé que les résultats sont bien plus homogènes à l’intérieur d’un groupe de recherche qu’entre différents groupes, où l’on observe une variation 200 fois plus importante des taux d’inhibition de croissance.2 Cela est sans doute dû à des différences dans les méthodes expérimentales, les techniques de pipetage et la qualité de l’équipement entre les différentes équipes de recherche. Chacun de ces facteurs implique que les cellules sont soumises à différents niveaux de stress, ce qui peut donner lieu à des variations de la viabilité des cellules, et réduire la reproductibilité des expériences. Les forces de cisaillement sont une source inévitable de stress qui s'exerce sur les cellules lors du pipetage, particulièrement si elles doivent passer par une pointe de pipette trop étroite ou à une vitesse trop élevée. Cette action peut induire des changements phénotypiques et comportementaux et peut entraîner, au final, des écarts de viabilité cellulaire. Par conséquent, l’équipe d’un laboratoire utilisant des pointes à embout large peut obtenir une meilleure viabilité cellulaire et des conclusions plus précises qu’une équipe effectuant ses cultures cellulaires à l’aide de pointes à embout standard.
Lorsqu'on travaille avec des pipettes mécaniques, l’angle de pipetage varie inévitablement d’un utilisateur à l’autre, tout comme la vitesse d’aspiration et de distribution - selon la rapidité de déplacement du piston - ce qui créée d’autres variations du niveau de stress. Des démarrages et arrêts soudains ou des mouvements désordonnés peuvent être à l’origine d’écarts qui peuvent passer inaperçus s’ils ne sont pas correctement documentés par les chercheurs à ce moment-là. Les pipettes électroniques permettent de définir et de consigner clairement les vitesses de pipetage et de mélange, minimisant ainsi les différences de technique entre les utilisateurs ou les étapes de pipetage. Associer des pointes à embout large à des pipettes électroniques peut apporter un meilleur contrôle sur les forces de biotransformation à l’ensemble des utilisateurs et aider ainsi à améliorer la viabilité cellulaire.
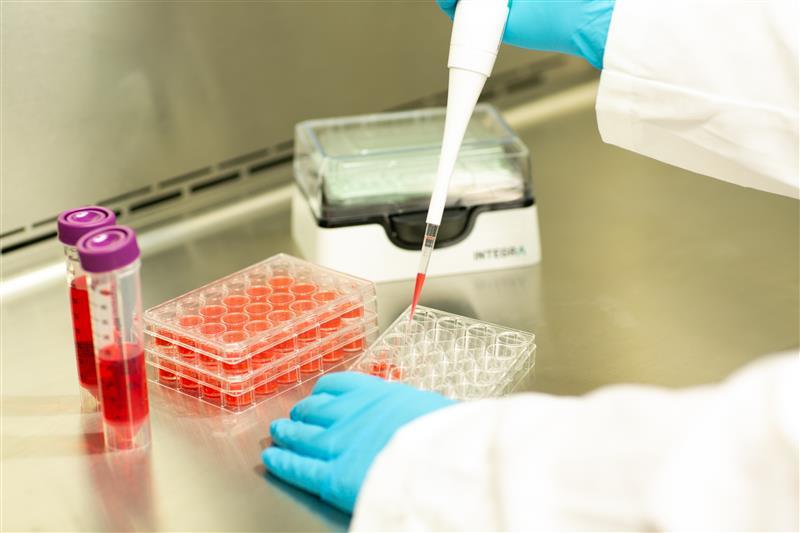
Les déviations par rapport aux protocoles
Pour obtenir une culture reproductible des cellules, les chercheurs doivent s'en tenir autant que possible aux protocoles décrits, le moindre écart pouvant générer des incohérences. Par exemple, des variations dans le nombre de cellules ensemencées ou dans la distribution des cellules dans le milieu peuvent entraîner une croissance cellulaire variable et impacter les résultats. Pour les essais de cytotoxicité par exemple, le nombre de cellules peut augmenter significativement la concentration minimale inhibitrice d’un antibiotique - un phénomène nommé ‘effet inoculum’ - il doit donc être constant. Un mélange régulier du milieu garantit que les cellules sont en suspension et réparties de manière égale dans la solution, empêchant ainsi la formation d’un gradient de concentration cellulaire entre le fond et le haut du récipient. Cette action doit être homogène d'une expérience à l'autre pour assurer une distribution et un ensemencement égaux des cellules. Toutefois, le fait de mélanger exerce une force de cisaillement sur les cellules qui peut générer un stress, le surmélange doit donc être évité pour prévenir les variations de viabilité des cellules. S'en tenir autant que possible au protocole et consigner précisément toutes les méthodologies, les étapes de mélange et les vitesses de pipetage peuvent aider à améliorer la reproductibilité des tâches de manipulation des cellules.

La contamination
La contamination biologique des échantillons par des micro-organismes et la contamination croisée entre différentes lignées cellulaires durant la manipulation des cellules peuvent impacter la santé des cellules et produire des résultats peu fiables. Non détectée, la contamination peut être à l’origine de conclusions erronées sur la capacité de survie et le comportement des cellules, compromettant l’intégrité et la reproductibilité des recherches. La manipulation correcte des échantillons de cellules, du milieu et des réactifs doit inclure des procédures et des équipements aseptisés - tels que des pipettes et des pointes stériles, l'utilisation de pointes à filtre et l'automatisation des opérations - afin de prévenir la contamination des échantillons, ainsi que des tests de contrôle-qualité efficaces pour détecter la présence éventuelle de micro-organismes indésirables.
Garantir des manipulations reproductibles
L’automatisation des flux de travail peut contribuer à améliorer la reproductibilité et le contrôle des forces de cisaillement sur les cellules, éliminant les variations inévitablement associées au traitement manuel. C’est particulièrement important quand on travaille avec un grand débit d’échantillons dans des plaques à 384 puits, ce qui est pratiquement irréalisable manuellement sans obtenir un taux bien plus élevé d’incohérence. Passer à des processus automatisés peut aider à éliminer cette variabilité, conférant un meilleur contrôle et une uniformité accrue des forces de biotransformation et de manipulation des cellules.3
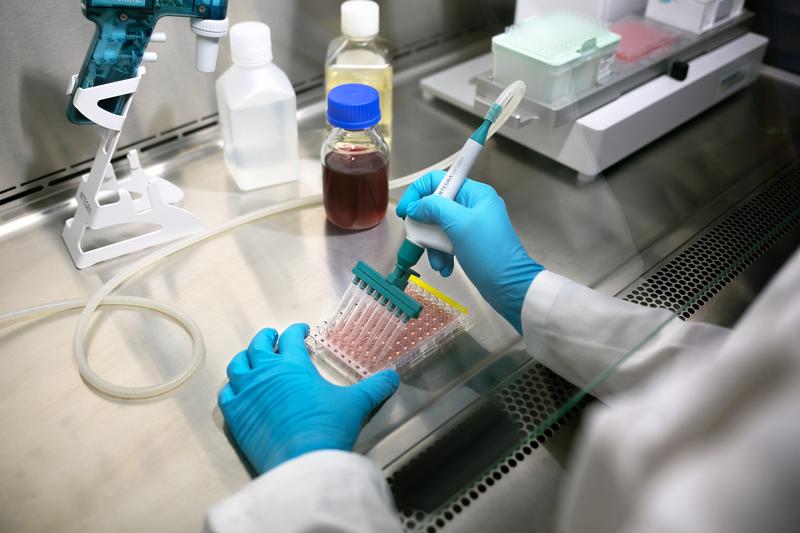
Idéalement, il faudrait automatiser chaque étape du pipetage en culture cellulaire - de l'ensemencement au traitement - afin de réduire les écarts liés aux utilisateurs, et les pipettes électroniques sont un moyen simple et abordable de commencer. Avec une pipette électronique, les utilisateurs peuvent sélectionner, documenter et enregistrer des protocoles de pipetage avec des vitesses de distribution et des routines de mélange définies, de sorte que chaque action soit effectuée à chaque fois à la même vitesse, quelles que soient l’expérience ou la technique de l’utilisateur. En outre, le mode Distribution répétée permet d’aspirer un grand volume de liquide et de le distribuer en petits volumes prédéfinis, réduisant les allers-retours entre la source et la plaque, qui sont autant de sources d’incohérences et d’erreurs de manipulation. A l'instar des pipettes électroniques, tous les contenants plastiques du laboratoire, pointes de pipettes inclues, doivent être cohérents, car les écarts dans la forme et la dimension des pointes, ainsi que dans le diamètre de l’orifice, peuvent induire des effets différents sur les cellules.
Aller un peu plus loin et automatiser la totalité du processus de pipetage à l'aide d'un robot permettrait d’éliminer complètement l'influence de la technique ou de l’expérience de l'utilisateur. Bien qu'une courbe d’apprentissage soit probable lors de la phase de transfert des techniques manuelles vers les processus automatisés - pour familiariser le personnel avec les nouveaux équipements et fournitures -, un flux de travail sans intervention élimine, au final, la source potentielle de variabilité et de contamination liée à l'utilisateur, augmentant ainsi la reproductibilité des techniques de manipulation.
- Baker, M (2016). Reproducibility crisis. Nature, 533(26), 353-66.
- Niepel, M., et al. (2019). A multi-center study on the reproducibility of drug-response assays in mammalian cell lines. Cell systems, 9(1), 35-48
- Brindley, D., et al. (2011). Bioprocess forces and their impact on cell behavior: implications for bone regeneration therapy. Journal of tissue engineering.