· 产品新闻
避免细胞培养污染的技巧贴士
对于所有的科学家而言,发现受污染的样本都意味着高昂的代价,因为昂贵的试剂和宝贵的研究时间都被浪费了,而更糟糕的情况则是整批样本都有可能作废。然而,如果未能发现污染,就有可能对细胞的行为和存活得出预期之外或者错误的结论。如果是在疫苗和生物药的研发过程中未能检测到污染,就有可能造成潜在的健康和安全风险。所有表面上的细胞培养条件都必须是可重复的,才能将基于细胞的疗法用作有效的工具,但如果存在着隐藏的污染影响,那么这就不可能实现。
隐藏的细胞污染风险
污染的后果可大可小,有时可能只会造成一些不便,比如需要处理掉一瓶受污染的细胞,而有时却可能造成更广泛的后果,比如发表了看似可信的结果,而实际上则是由于未发现的交叉污染所导致的错误结论。据估计,超过15%的细胞培养研究是基于错误识别或者受到交叉污染的细胞系展开的,这些污染可能完全检测不到,严重影响了结果的可重复性和准确性。1 例如,某些污染可能影响细胞的行为(包括代谢和生长),如果未检测到,就可能让您错误的认为鉴定出了新的细胞系或未曾被发现的新的先天行为。因此,我们对于细胞培养的很多预期和观点可能都基于错误的信息,来自于没有正确鉴别的细胞系。
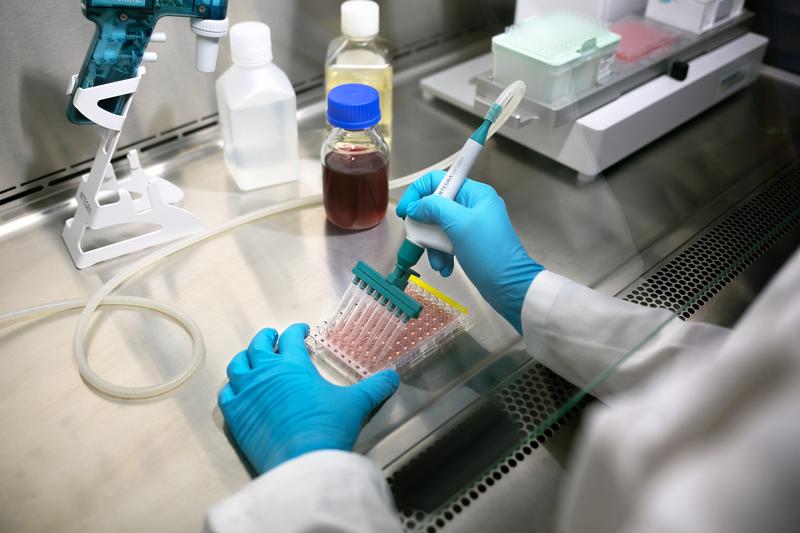
生物污染
令人惊讶的是,据报道,生物污染的发生率要比想象中的高得多,因为大多数反复出现的问题都被认为来自于微生物。2 不幸的是,培养健康细胞所需的条件(比如营养丰富的培养基以及受控的温度)也是适合某些有害微生物生长和增殖的完美环境。样本的生物污染可以看作是一种新发疾病的体外等同版本,有时,伴随着入侵微生物的生长和复制,细胞必须竞争关键的营养物质,并保护自身不受有毒副产物的侵害,3 而有些污染物则能够吞噬整个细胞。除此之外,已经证实,支原体污染物会改变基因表达以破坏重要的细胞通路。4 这将对细胞活力产生极大的影响,造成细胞状态不佳和死亡。感染在肉眼甚至显微镜下的可见程度往往决定了其未被发现的可能性。以下是几种需要避免的常见污染物,以及识别它们的方法:
- 细菌 – 细菌感染通常会使细胞看起来特别不健康,引起培养基浊度或颜色的迅速变化。可移动的细菌在显微镜下可见。
- 真菌 – 真菌污染,比如霉菌和酵母菌,通常会在培养基中形成清晰可见的结构,肉眼或在显微镜下即可检查。
- 支原体 – 支原体是最小的独立生存生物,即使在显微镜下也通常不可见。它们缺乏细胞壁,因此不受抗生素活性的影响。专项的检测,比如PCR或DNA荧光染色,是检测这类污染的方法。
无菌工作技术和无菌环境有助于降低细胞生物污染的风险。受损的细胞样本或试剂必须进行正确的处置,即便只是轻微的污染(比如在通风橱下打开一个含有空气传播微生物的烧瓶),都要求对整个环境进行去污染处理,以避免微粒的沉降。针对污染物的专项检测以及常规的显微镜观察,应该成为所有细胞培养工作流程中的标准质量控制筛查程序。此外,FDA积极地鼓励生物制药厂商进行细胞基质的质量检测。5
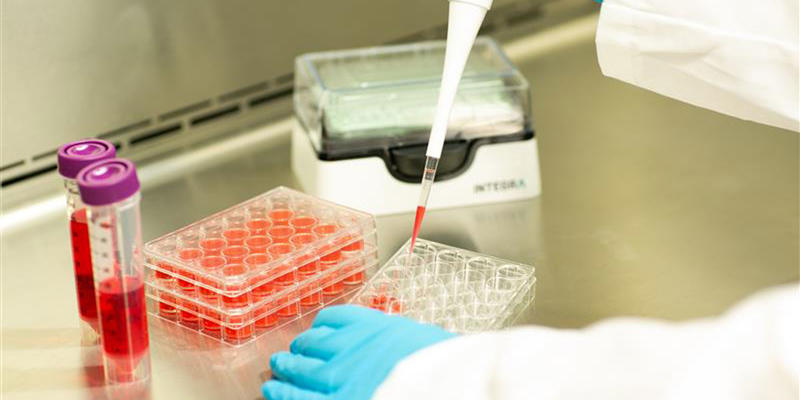
完善装备以避免污染
不幸的是,要彻底消除一切污染源几乎是不可能的,但可以采用各种无菌规程来最大程度的减少污染的发生——从使用正确的工具开始。以下是一些关于选择正确的移液器和枪头以及细胞培养工作流程的适当操作的建议:
- 细胞培养过程应始终使用无菌移液器和枪头。购买的枪头应附带无菌声明,以减轻对生物污染的担忧。
- 应使用带滤芯的枪头以避免吸取时形成的气溶胶进入移液器腔内,否则将可能会对未来移取的样本造成交叉污染。
- 每支枪头都应该与移液器形成完美的密封,并且不渗漏或脱落。这可以避免液体溢出或滴落在工作台上,造成污染其他样本或实验室工作人员的风险。
- 正确的移液规程应该包含预湿润步骤。在移取目标样本之前,全量程吸取同种液体后排出通常是良好的移液实践,这能够平衡枪头内的环境并降低枪头滴液的风险。
- 自动化是降低源自使用者的污染风险的较佳解决方案,因为它无需手动操作。它还有助于减少人为错误并降低细胞系交叉污染的可能性,优化工作的可重复性。理想条件下,自动化装置应该处在良好维护的超净工作台的保护之下,并进行频繁的清洁程序。
了解INTEGRA如何帮助您优化细胞培养操作。
References
- Nardone, R. M. (2008). Curbing rampant cross-contamination and misidentification of cell lines. Biotechniques, 45(3), 221-227.
- Langdon, S. P. (2004). Cell culture contamination. Cancer Cell Culture, 309-317.
- Lincoln, C. K., & Gabridge, M. G. (1998). Cell culture contamination: sources, consequences, prevention, and elimination. Methods in cell biology, 57, 49-65.
- Chernov, V. M., Chernova, O. A., & Sanchez-Vega, J. T. (2014). Mycoplasma contamination of cell cultures: vesicular traffic in bacteria and control over infectious agents. Acta Naturae (англоязычная версия), 6(3 (22)).
- U.S. Department of Health and Human Services. (2018). Food and Drug Administration. Elimination of the 21 CFR 610.30 Test for Mycoplasma, 1-6.