Tipps zum Verhindern von Kontaminationen in der Zellkultur
Kontaminierte Proben sind immer eine kostspielige Angelegenheit, weil damit nicht nur wertvolle Reagenzien und Forschungszeit verloren gehen, sondern schlimmstenfalls eine ganze Charge unbrauchbar sein kann. Wenn eine Kontamination allerdings unentdeckt bleibt, kann sie unerwartete oder falsche Schlussfolgerungen über das Verhalten und die Überlebensrate von Zellen nach sich ziehen. Wenn eine Kontamination bei der Erforschung und Entwicklung von Impfstoffen und Biopharmaka unerkannt bleibt, kann dies zur Gefährdung von Gesundheit und Sicherheit führen. Um wirksame Behandlungen herzustellen, müssen alle äußeren Bedingungen der Zellkultivierung reproduzierbar sein; im Fall einer unerkannten Kontamination ist dies jedoch nicht möglich.
Das verborgene Risiko der Kontamination von Zelllinien
Eine Kontamination kann kleinere Unannehmlichkeiten verursachen, etwa wenn ein verunreinigtes Zellgefäß entsorgt werden muss; sie kann aber auch von großer Tragweite sein, beispielsweise wenn Ergebnisse veröffentlicht werden, die durch eine unerkannte Kreuzkontamination verfälscht wurden. Schätzungen zufolge stützen sich über 15 % aller Zellkulturstudien auf falsch identifizierte oder durch Kreuzkontamination verunreinigte Zelllinien, wodurch die Reproduzierbarkeit und Präzision der Ergebnisse beeinträchtigt wird.1 So können Kontaminationen beispielsweise das Verhalten von Zellen, einschließlich Stoffwechsel und Wachstum, beeinflussen und, wenn sie nicht erkannt werden, zu der falschen Schlussfolgerung führen, dass eine neue Zelllinie oder ein neues inhärentes Verhalten entdeckt wurde. Es ist demnach möglich, dass sich viele unserer auf Zellkulturen beruhenden Voraussagen und Überzeugungen auf falsche Informationen stützen, die von nicht korrekt authentifizierten Zelllinien stammen.
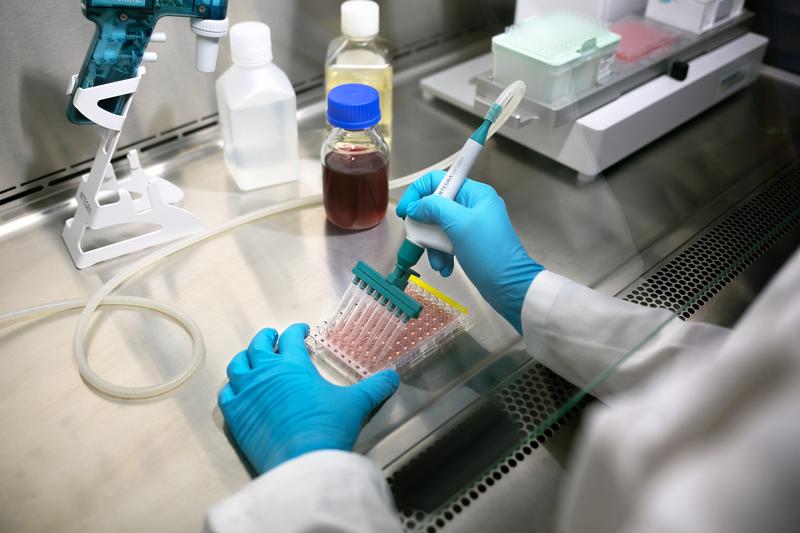
Biologische Kontamination
Fälle biologischer Kontamination sind sogar noch weitaus häufiger, denn es wird davon ausgegangen, dass die meisten wiederkehrenden Probleme mikrobiellen Ursprungs sind.2 Leider sind die Bedingungen für eine erfolgreiche Zellkultivierung – nährstoffreiches Medium und kontrollierte Temperatur – auch die perfekte Umgebung für Wachstum und Proliferation unerwünschter Mikroorganismen. Man kann die biologische Kontamination von Proben als das In-vitro-Pendant einer neu auftretenden Krankheit beschreiben; manchmal müssen Zellen um wesentliche Nährstoffe konkurrieren und sich gegen toxische Nebenprodukte verteidigen, wenn mikrobielle Eindringlinge wachsen und sich vermehren3, während andere Kontaminanten ganze Zellen verschlingen können. Darüber hinaus ist erwiesen, dass Mykoplasmen-Kontaminationen Veränderungen in der Genexpression verursachen und wichtige Zellwege stören.4 Dies hat enorme Folgen für die Viabilität der Zellen und führt zu schlechter Zellgesundheit und Zelltod. Wie wahrscheinlich es ist, dass eine Infektion unerkannt bleibt, hängt in der Regel davon ab, wie gut sie mit bloßem Auge oder auch unter dem Mikroskop zu sehen ist. Hier einige gängige Kontaminanten, die es zu vermeiden gilt, und Hinweise zu ihrer Erkennung:
- Bakterien: Eine bakterielle Infektion führt in der Regel dazu, dass Zellen ungesund aussehen, und verursacht eine rasche Trübung oder Farbveränderung des Mediums. Eventuell lassen sich mit dem Mikroskop auch Bakterienbewegungen beobachten.
- Pilze: Pilze als Kontaminanten, z. B. Schimmel oder Hefen, bilden oft deutlich sichtbare Strukturen im Medium, die mit bloßem Auge oder unter dem Mikroskop unschwer zu erkennen sind.
- Mykoplasmen: Mykoplasmen sind die kleinsten aller frei lebenden Organismen und in der Regel nicht einmal unter dem Mikroskop sichtbar. Da sie zudem keine Zellwand haben, sind sie immun gegen Antibiotika. Die einzige Möglichkeit zur Erkennung solcher Kontaminationen sind spezifische Tests, etwa PCR oder fluoreszierende DNA-Färbung.
Aseptische Arbeitstechniken und sterile Umgebungen können dazu beitragen, die Gefahr einer biologischen Zellkontamination zu mindern. Verunreinigte Zellproben oder Reagenzien müssen ordnungsgemäß entsorgt werden, und auch bei einer geringfügigen Kontamination – etwa wenn ein Gefäß, das luftgetragene Mikroorganismen enthält, in einer Sicherheitswerkbank geöffnet wurde – muss die gesamte Umgebung dekontaminiert werden, um zu verhindern, dass einzelne Partikel sich absetzen. Neben regelmäßigen mikroskopischen Betrachtungen sollten bei allen Arbeitsabläufen, bei denen Zellkulturen zum Einsatz kommen, spezifische Tests auf Kontaminanten Teil des Standardverfahrens zur Qualitätskontrolle sein. Darüber hinaus fordert die FDA die Hersteller von Biopharmaka nachdrücklich dazu auf, die Qualität ihrer Zellsubstrate zu testen.5
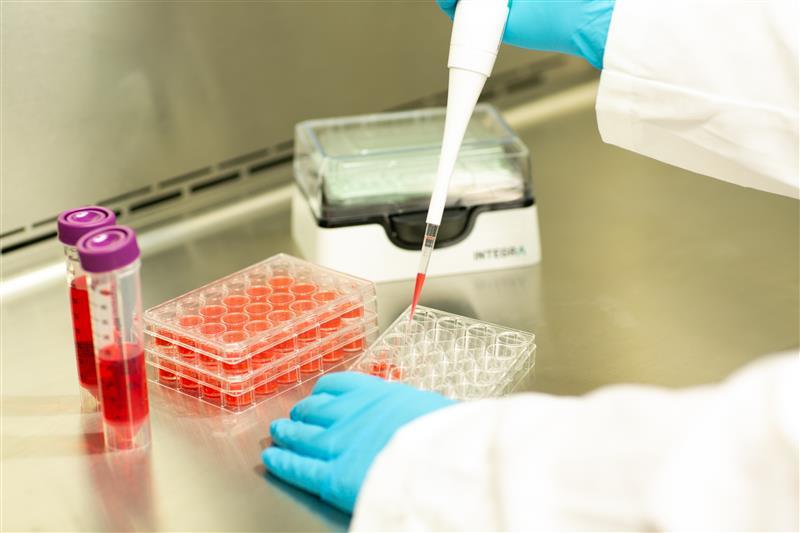
Verhindern von Kontamination durch die richtige Ausrüstung
Leider ist es nahezu unmöglich, alle Kontaminationsquellen vollständig auszuschalten; mithilfe verschiedener aseptischer Verfahren, angefangen bei der Verwendung der richtigen Instrumente, lassen sich Verunreinigungen jedoch auf ein Minimum reduzieren. Hier einige Empfehlungen für die Auswahl der richtigen Pipetten und Pipettenspitzen und die ordnungsgemäße Handhabung von Zellkulturen:
- In Verbindung mit Zellkulturen sind immer sterile Pipetten und Spitzen zu verwenden. Die Spitzen sollten beim Kauf mit einer Sterilitätsauszeichnung versehen sein, damit keine Sorge um eine mögliche biologische Kontamination aufkommen kann.
- Um zu vermeiden, dass beim Aspirieren Aerosole in den Pipettenzylinder gelangen, was eine Kreuzkontamination der Zelllinien durch künftige Proben hervorrufen könnte, sollten Filterspitzen verwendet werden.
- Spitzen sollten perfekt auf die Pipette passen, so dass sie nie abfallen oder undicht sind. Dadurch wird die Verunreinigung von Labortischen verhindert, die zur Kontamination anderer Proben oder von Laborpersonal führen könnte.
- Nach Aufstecken der Pipettenspitzen wird empfohlen, das maximale Volumen 3x zu aspirieren und zu dispensieren bevor mit dem Pipettieren begonnen wird. Dies gleicht Temperaturunterschiede aus und befeuchtet den Luftraum innerhalb der Spitze, wodurch die Tropfgefahr verringert wird.
- Da die Automatisierung einen vollständig kontaktfreien Arbeitsablauf ermöglicht, ist sie die optimale Lösung, um das Risiko einer anwenderbedingten Kontamination auszuschalten. Sie trägt zudem dazu bei, menschliche Fehler und die Wahrscheinlichkeit der Kreuzkontamination von Zelllinien zu senken, und verbessert somit die Reproduzierbarkeit von Aufgaben. Im Idealfall sollte eine automatisierte Anlage durch eine gut gepflegte Sicherheitswerkbank geschützt und häufig gereinigt werden.
Informieren Sie sich, wie INTEGRA Ihr Zellkulturhandling verbessern kann.
Weitere Artikel: An introduction to cell culture and its challenges
Literaturangaben
- Nardone, R. M. (2008). Curbing rampant cross-contamination and misidentification of cell lines. Biotechniques, 45(3), 221-227.
- Langdon, S. P. (2004). Cell culture contamination. Cancer Cell Culture, 309-317.
- Lincoln, C. K., & Gabridge, M. G. (1998). Cell culture contamination: sources, consequences, prevention, and elimination. Methods in cell biology, 57, 49-65.
- Chernov, V. M., Chernova, O. A., & Sanchez-Vega, J. T. (2014). Mycoplasma contamination of cell cultures: vesicular traffic in bacteria and control over infectious agents. Acta Naturae (англоязычная версия), 6(3 (22)).
- U.S. Department of Health and Human Services. (2018). Food and Drug Administration. Elimination of the 21 CFR 610.30 Test for Mycoplasma, 1-6.