Conseils pour prévenir la contamination dans la culture cellulaire
La découverte d’échantillons contaminés est coûteuse pour tout scientifique de par la perte d’un temps de recherche et de réactifs précieux, et dans le pire des cas, le gaspillage de lots entiers. Non détectée, la contamination peut donner lieu à des conclusions inattendues ou inexactes sur le comportement et la survie des cellules. Cela peut induire un risque potentiel de santé et de sécurité si la contamination reste indétectée dans la recherche et le développement de vaccins et de biopharmaceutiques. Toutes les conditions apparentes de la culture cellulaire doivent être reproductibles pour que les thérapies cellulaires soient des outils efficaces, mais cela n’est pas possible du fait de l’influence cachée de la contamination.
Le risque caché de contamination cellulaire
Les conséquences de la contamination vont d’inconvénients mineurs, tels que la nécessité de jeter un flacon de cellules contaminé, à des impacts nettement plus graves, comme la publication de résultats supposément fiables, mais en réalité inexacts du fait d’une contamination croisée non détectée. On estime que plus de 15 % des études de culture cellulaire se basent sur des lignées cellulaires mal identifiées ou ayant fait l’objet d’une contamination croisée sans que cela ait été identifié, compromettant ainsi la reproductibilité et l’exactitude des résultats.1 Par exemple, certaines incidences peuvent influencer le comportement des cellules – y compris le métabolisme et la croissance – et, si elles ne sont pas détectées, vous faire faussement croire que vous avez identifié une nouvelle lignée cellulaire ou découvert un nouveau comportement inné. En conséquence, nombre de nos prédictions et croyances en matière de culture cellulaire peuvent être basées sur de fausses informations, à partir de lignées cellulaires sans authentification correcte.
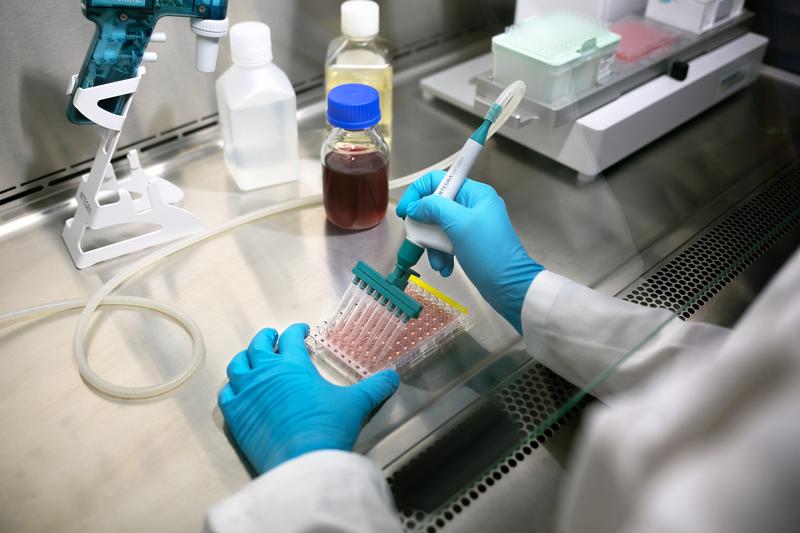
La contamination biologique
Étonnamment, les incidences des contaminations biologiques sont apparemment très fréquentes, les problèmes revenant le plus souvent étant généralement d’origine microbienne.2 Malheureusement, les conditions nécessaires à la culture de cellules saines – comme un milieu riche en nutriments et des températures contrôlées – sont également un environnement parfait pour la croissance et la prolifération de certains micro-organismes indésirables. La contamination biologique d’échantillons peut être décrite comme l’équivalent in vitro d’une maladie émergente ; les cellules doivent parfois se disputer les nutriments essentiels et se défendre contre des sous-produits toxiques quand des microbes invasifs croissent et se répliquent,3 tandis que certains contaminants peuvent engloutir des cellules entières. En outre, il est prouvé que les contaminants mycoplasmiques modifient l’expression des gènes et perturbent d’importantes voies cellulaires.4 Cela a un impact considérable sur la viabilité des cellules, résultant dans la mauvaise santé et la mort cellulaire. Le degré de visibilité d’une infection à l’œil nu, ou même au microscope, détermine souvent son niveau de probabilité à rester indétectée. Voici quelques contaminants usuels à éviter et comment les identifier :
- Bactéries – Lors d’une infection bactérienne, les cellules ont généralement l’air en mauvaise santé, avec un rapide changement de turbidité ou de couleur du milieu. Les bactéries en mouvement peuvent également être visibles au microscope.
- Champignons – Les contaminants fongiques, moisissures et levures par exemple, se développent souvent en structures clairement visibles dans le milieu, facilement repérables à l’œil nu ou au microscope.
- Mycoplasmes – Les mycoplasmes sont les plus petits des organismes vivants indépendants et ne sont généralement pas visibles, même au microscope. Sans paroi cellulaire, ils sont par conséquent insensibles aux antibiotiques. Seul un dépistage spécifique, via la PCR ou la coloration de l’AND par fluorescence, permet de détecter une contamination.
Des techniques de travail aseptisées et des environnements stériles peuvent contribuer à réduire le risque de contamination biologique des cellules. Les échantillons de cellules ou les réactifs contaminés doivent être éliminés correctement et il faut, même dans le cas d'une contamination mineure – comme l’ouverture d’un seul flacon contenant des micro-organismes aéroportés sous une hotte à flux laminaire –décontaminer tout l’environnement pour prévenir la colonisation des particules. Un dépistage spécifique des contaminants ainsi que des observations microscopiques régulières devraient être mis en oeuvre comme procédure de dépistage standard pour le contrôle qualité de tous les processus de culture cellulaire. Par ailleurs, la FDA encourage activement les fabricants de produits biopharmaceutiques à tester la qualité des substrats cellulaires.5
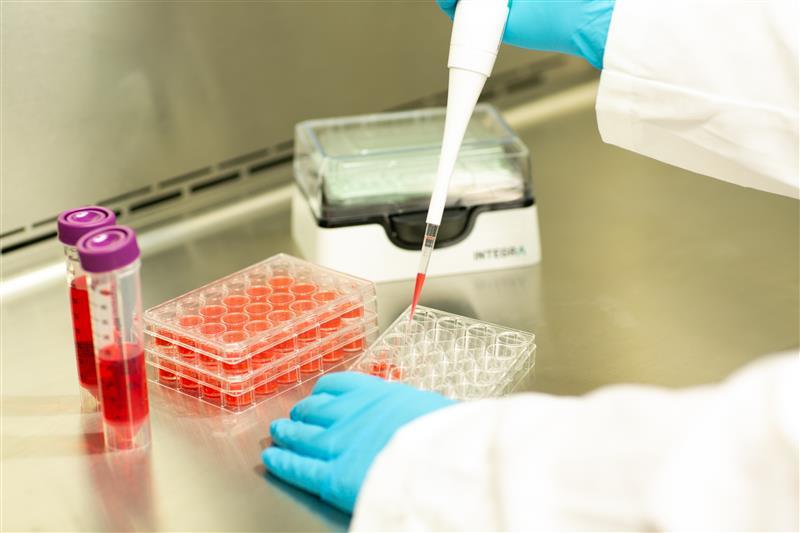
S’équiper pour prévenir la contamination
S’il est malheureusement quasiment impossible d’éliminer complètement toutes les sources de contamination, diverses procédures d’aseptisation peuvent être adoptées pour minimiser le risque – à commencer par l’utilisation des outils appropriés. Voici quelques suggestions pour bien sélectionner les pipettes et les pointes et effectuer les manipulations adéquates dans les processus de culture cellulaire :
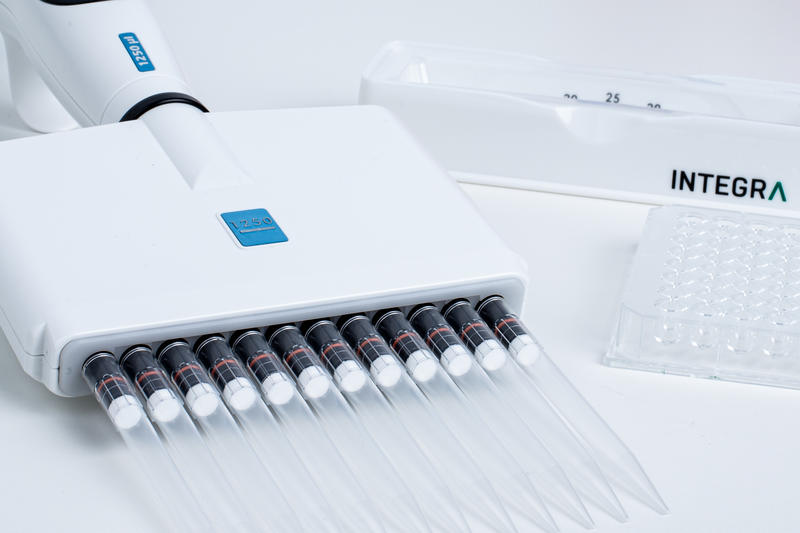
- Il faut toujours utiliser des pipettes et des pointes stériles pour la culture cellulaire. Lors de l’achat, les pointes doivent être accompagnées d’une déclaration de stérilité, de façon à éviter tout risque de contamination biologique.
- Des pointes à filtre doivent être utilisées pour empêcher les aérosols créés lors de l’aspiration de pénétrer dans le corps de la pipette, ce qui pourrait entraîner une contamination croisée des lignées cellulaires pour de prochains échantillons.
- Chaque binôme pointe/pipette doit présenter une étanchéité parfaite, et la pointe ne doit jamais fuir ni tomber. Cela empêche le liquide de se déverser ou de goutter sur la paillasse, risquant ainsi de contaminer d’autres échantillons ou le laborantin.
- Les procédures de pipetage adéquates doivent inclure des techniques de pré-humidification. Aspirer et éjecter tout le volume de la pipette avec le liquide avant de pipeter l'échantillon est généralement une bonne pratique, de façon à équilibrer l’environnement de la pointe et à réduire le risque de pointe qui goutte.
- L’automatisation est la meilleure solution pour réduire le risque de contamination de la part de l’utilisateur, puisqu’elle permet un fonctionnement mains-libres. Elle contribue aussi à réduire l’erreur humaine et la probabilité de contamination croisée des lignées cellulaires, pour une meilleure reproductibilité des tâches. Dans l’idéal, le système d’automatisation doit être protégé par une hotte à flux laminaire soigneusement entretenue et soumise à de fréquentes procédures de nettoyage.
Découvrez comment INTEGRA peut vous aider à améliorer vos manipulations de culture cellulaire.
Lecture complémentaire : An introduction to cell culture and its challenges
References
- Nardone, R. M. (2008). Curbing rampant cross-contamination and misidentification of cell lines. Biotechniques, 45(3), 221-227.
- Langdon, S. P. (2004). Cell culture contamination. Cancer Cell Culture, 309-317.
- Lincoln, C. K., & Gabridge, M. G. (1998). Cell culture contamination: sources, consequences, prevention, and elimination. Methods in cell biology, 57, 49-65.
- Chernov, V. M., Chernova, O. A., & Sanchez-Vega, J. T. (2014). Mycoplasma contamination of cell cultures: vesicular traffic in bacteria and control over infectious agents. Acta Naturae (англоязычная версия), 6(3 (22)).
- U.S. Department of Health and Human Services. (2018). Food and Drug Administration. Elimination of the 21 CFR 610.30 Test for Mycoplasma, 1-6.