· 製品ニュース
細胞培養における汚染防止のヒント
サンプルの汚染が発見された場合、貴重な試薬や研究時間が失われ、最悪の場合はバッチ全体が台無しになる可能性があるため、研究者にとって痛手となります。しかしながら汚染が検出されない場合、細胞の挙動と生存について予期しないまたは不正確な結論が汚染により導き出される可能性があります。ワクチンやバイオ医薬品の研究開発で汚染が検出されない場合、これは潜在的な健康と安全のリスクをもたらす可能性があります。細胞ベースの治療法を効果的なツールとして使用するには、明らかな細胞培養条件をすべて再現できるようにする必要がありますが、汚染の影響が明らかでない場合は再現することはできません。
細胞汚染の隠れたリスク
汚染による影響は、汚染した細胞の入ったフラスコは処分する必要があるなど多少不便なことから、信頼性が高いと想定されていた結果が、検出されなかったクロスコンタミネーションによって不正確になることを公表するなどさまざまです。細胞培養研究の15%以上が、誤認またはクロスコンタミネーションが起きたにもかかわらず、全く検出されていない細胞株に基づいており、再現性 と結果の精度が損なわれると推定されています1。例えば、これらの中には、代謝や増殖など細胞の挙動に影響を及ぼす可能性があるものもあり、検出されない場合、研究者は、新しい細胞株を同定、または新しい生得的な挙動を発見したと誤って信じてしまう可能性があります。したがって、細胞培養に関する私たちの予測と信念の多くは、正しく証明されていない細胞株から得た誤った情報に基づいている可能性があります。
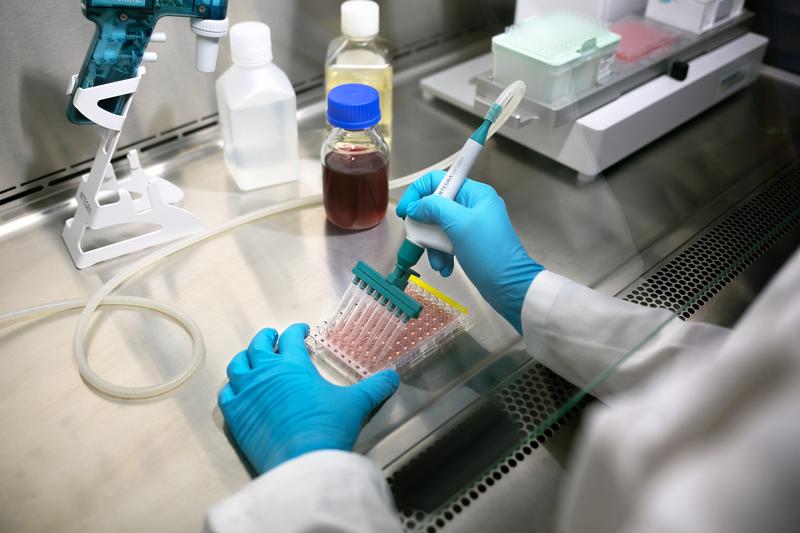
生物学的汚染
驚くべきことに、生物学的汚染の発生ははるかに多いと報告されています。これは、繰り返し起こるほとんどの問題が微生物に起因するものだと予想されるためです2。残念ながら、栄養豊富な培地や制御された温度など、健康な細胞を培養するために必要な条件は、一部の不要な微生物の成長と増殖に最適な環境でもあります。サンプルの生物学的汚染は、in vitroでの新興感染症と同等なものとして説明することができます。侵入する微生物が成長して複製するため、細胞は、必須栄養素を求めて競争し、有毒な副産物から身を守らなければならないことがあります3。一方で、汚染物質の中には細胞全体を飲み込む可能性があるものもあります。さらに、マイコプラズマ汚染は、遺伝子発現を修正して重要な細胞経路を破壊することが証明されています4。これは、細胞の生存率 に大きな影響を及ぼし、細胞の健康状態を悪化させ、死に至らしめます。感染が肉眼あるいは顕微鏡下で、どれだけ目視可能であるかによって、感染が検出されない可能性がでてくることがよくあります。ここでは、回避するべき一般的な汚染物質とそれらを特定する方法の一部を紹介します。
- 細菌—細菌感染では通常、細胞が著しく不健康な状態になり、培地の濁度や色が急速に変化します。また、動く細菌も顕微鏡を通して見ることができます。
- 真菌—カビや酵母菌などの真菌汚染物質は、培地中ではっきりと見える構造に成長することが多く、肉眼または顕微鏡で簡単に検出できます。
- マイコプラズマ—マイコプラズマはすべての自由生活生物の中で最も小さく、顕微鏡下でも通常は見えません。また、それらは細胞壁を欠いているため、抗生物質の活性に免疫があります。PCRや蛍光DNA染色などの特定の検査は、汚染を検出する唯一の方法です。
無菌操作技術と無菌環境は細胞の生物学的汚染リスクを軽減します。損なわれた細胞サンプルや試薬は正しく廃棄しなければならず、層流下で浮遊微生物が入ったのフラスコを開栓するなどのわずかな汚染の発生においても、粒子が定着するのを防ぐために環境全体を除染する必要があります。特定の汚染物質の検査は、定期的な顕微鏡観察とともに、すべての細胞培養ワークフローの標準的な品質管理スクリーニング法として採用します。さらに、FDAは、バイオ医薬品メーカーに対し、細胞基材の品質評価をするための試験を積極的に奨励しています5。
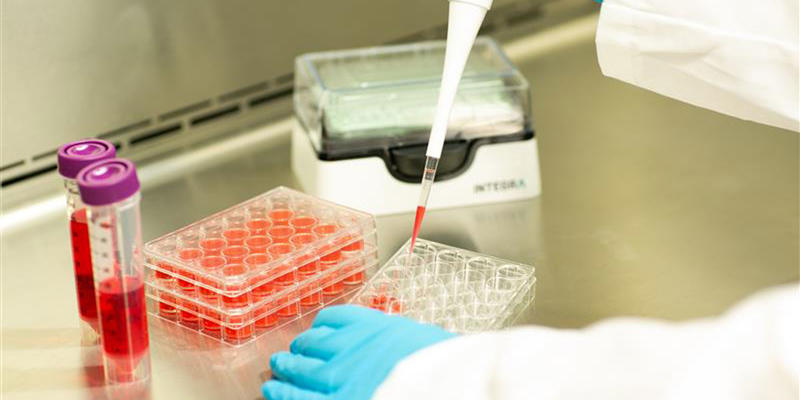
汚染を防ぐための装備を整える
残念ながら、すべての汚染源を完全に排除することはほぼ不可能ですが、適切なツールを使用することから始めて、発生を最小限に抑えるために採用できるさまざまな無菌操作があります。ここでは、正しいピペットとチップの選択方法および細胞培養ワークフローにおける適切な操作方法をいくつか紹介します。
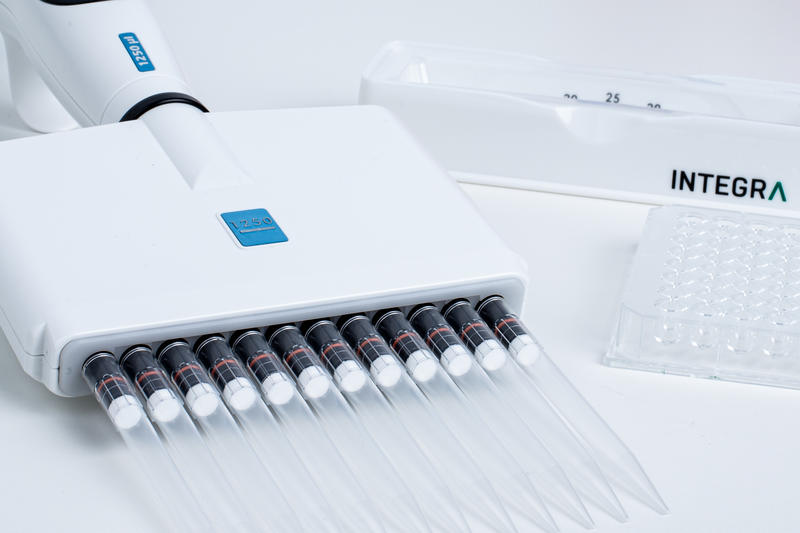
- 滅菌ピペットとチップは細胞培養に使用します。生物学的汚染の懸念を軽減するために、チップには購入時に滅菌証明書が必要になります。
- 吸引中に発生したエアロゾルがピペットのバレルに入ると、今後使用するサンプルで細胞株のクロスコンタミネーションが発生する可能性があります。これを防ぐために、フィルターチップを使用します。
- すべてのチップはピペットに確実に装着され、漏れたり落下したりしないようにしなければなりません。これにより、液体がワークベンチにこぼれたり滴り落ちたりして、他のサンプルやラボの技術者を汚染するリスクがなくなります。
- 適切な分注操作には、プレウェット手順を含める必要があります。サンプルを分注する前に、ピペット全量の液体を吸引して排出するプリウェッット手順は、チップ環境を均質化し、チップ先端からの滴漏れのリスクを低減するために一般的に適切とされる分注操作です。
- 自動化は、ハンズフリーで行われるため、ユーザーによる汚染のリスクを軽減するための最良のソリューションです。また、ヒューマンエラーや細胞株のクロスコンタミネーションの可能性を減らし、作業の再現性を向上させます。理想的には、自動化のセットアップは、手入れの行き届いた層流キャビネットによって保護され、頻繁に洗浄する必要があります。
INTEGRAが細胞培養処理の向上をいかに支援できるかをぜひご覧ください。
参考文献
- Nardone, R. M. (2008). Curbing rampant cross-contamination and misidentification of cell lines. Biotechniques, 45(3), 221-227.
- Langdon, S. P. (2004). Cell culture contamination. Cancer Cell Culture, 309-317.
- Lincoln, C. K., & Gabridge, M. G. (1998). Cell culture contamination: sources, consequences, prevention, and elimination. Methods in cell biology, 57, 49-65.
- Chernov, V. M., Chernova, O. A., & Sanchez-Vega, J. T. (2014). Mycoplasma contamination of cell cultures: vesicular traffic in bacteria and control over infectious agents. Acta Naturae (англоязычная версия), 6(3 (22)).
- U.S. Department of Health and Human Services. (2018). Food and Drug Administration. Elimination of the 21 CFR 610.30 Test for Mycoplasma, 1-6.