· 製品ニュース
抗微生物薬耐性試験のための分子診断をスピードアップさせる
微生物は、抗生物質を過剰使用または誤用すると、時間の経過とともに抗微生物薬に対する遺伝的耐性を獲得する場合があり、その結果、一般的な感染症が治療困難となり、致死的となることもあります。近年、抗微生物薬耐性(AMR)に起因する疾病と死亡の割合が世界中で急速に上昇しているため、多剤耐性(MDR)病原体は重要な健康問題として注目されています。そのため、現在診断は、疾患の発症直後から抗生物質の不適切な処方を防ぐことによって治療の成功を増やし、患者の転帰を改善させるために、薬剤耐性を迅速かつ正確に識別することに重点を置いています。
抗微生物薬感受性試験への従来のアプローチ
最小発育阻止濃度(MIC)試験は、病原体の抗微生物薬感受性の測定によく使用されます。 これは、液体希釈法、寒天希釈法、抗微生物薬濃度勾配法、またはディスク拡散法によって測定することができます。これらの方法については、抗微生物薬感受性に関する情報提供ブログで詳しく説明されています。 これらの表現型解析法には確かに利点がありますが、欠点もいくつかあります。例えば、単調で時間がかかり、エラーが発生しやすい手動分注作業が必要なことが挙げられます。これによって、研究室のワークフローが大幅にペースダウンし、所要時間が長くなります。
INTEGRA Biosciencesの自動分注装置のラインアップは、これらの面倒な分注作業を大幅にスピードアップできるため、MIC試験を手動で行う場合に比べてスループットを高め、結果が出るまでの時間を短くします。当社のアプリケーションノートの自動最小発育阻止濃度試験は、特に液体希釈法に重点を置いています。このアプリケーションノートは、ASSIST PLUS分注ロボットをVOYAGERチップ間隔可変電動ピペットと併用して、正確度、精密度、再現性の高い結果を得るために、一定のピペット操作の高さ、速度、混合パラメーターを維持しながら、移動や混合の工程を自動化する詳細なガイドを提供しています。MIC試験の段階希釈に関するINTEGRAの自動分注ソリューションについての詳細はこちらをご確認ください。

AMRとの戦いにおける新戦術としての分子診断
分子診断法は、代替アプローチ、または従来法の補完を目的として、病原体やそれらの耐性メカニズムの両方を識別するための最適ツールとして浮上しつつあります。遺伝子型検査は、クラシックな培養ベースのアッセイよりも精度・正確度が高い傾向があります。この検査では病原体の単離および培養が必要ないため、結果がわずか1時間で得られる、より迅速な検査方法です。
遺伝子型法は、特定の耐性遺伝子や新規変異が発生していればそれらも直接検出でき(表1)、増幅ベース、シーケンスベース、ハイブリダイゼーションベースという3つのカテゴリーのうちの1つに分類される傾向があります。最初の2つの方法、増幅ベースとシーケンスベースについて詳しく説明しましょう。
多剤耐性生物 |
耐性マーカー遺伝子 |
|---|---|
| メチシリン耐性黄色ブドウ球菌(MRSA) | mecA |
|
基質特異性拡張型ベータラクタマーゼ(ESBLs): 大腸菌、肺炎桿菌 |
blaTEM blaSHV blaCTX-M |
|
カルバペネム耐性腸内細菌科細菌(CRE): 大腸菌、エンテロバクター・アエロゲネス、エンテロバクター・クロアカコンプレックス、肺炎桿菌、クレブシエラ・オキシトカ |
blaKPC blaOXA-48-like blaNDM blaIMP blaVIM |
|
バンコマイシン耐性腸球菌(VRE): エンテロコッカス・フェカリス、エンテロコッカス・フェシウム |
vanA vanB |
|
多剤耐性結核(MDR-TB): 結核菌群 |
katG inhA rpoB |
表1:一般的なMDR病原体とそれらの耐性マーカー遺伝子の例。
増幅ベース法
この方法の一例は、標的遺伝子配列を増幅して検出可能にする、一般的に使用される核酸ベース増幅法(NAAT)です。最も広く使用されているNAAT法は、ポリメラーゼ連鎖反応(PCR)です。リアルタイムPCR(またはqPCR)は、迅速で定量的な標的固有の結果が得られ、マルチプレックスパネルを使用して複数の耐性マーカー遺伝子を同時に特定できる臨床現場即時検査の状況において、特にMDR病原体の検出に役立ちます。
NAATワークフローには、マルチチャンネルピペットまたは自動化によってスループットを向上させるのに適した段階がいくつかあります。当社は、NAATワークフローのスループットを向上させるためのさまざまなソリューションを提供しており、例えば、MINI 96ポータブル電動ピペットは、96のサンプルまたは試薬を並行して添加することによって、迅速なサンプル抽出、qPCRのセットアップに使用できます。代わりにASSIST PLUS分注ロボットを使用すると、核酸抽出プロセスを自動化することができ、サンプルから高品質のDNA材料を一定に得ることが可能です。PCRサンプル調製のワークフロー全体を、ASSIST PLUS分注ロボット上で自動的に行うことができるため、手作業の時間をさらに短縮し、研究室全体のスループットを向上させることができます。
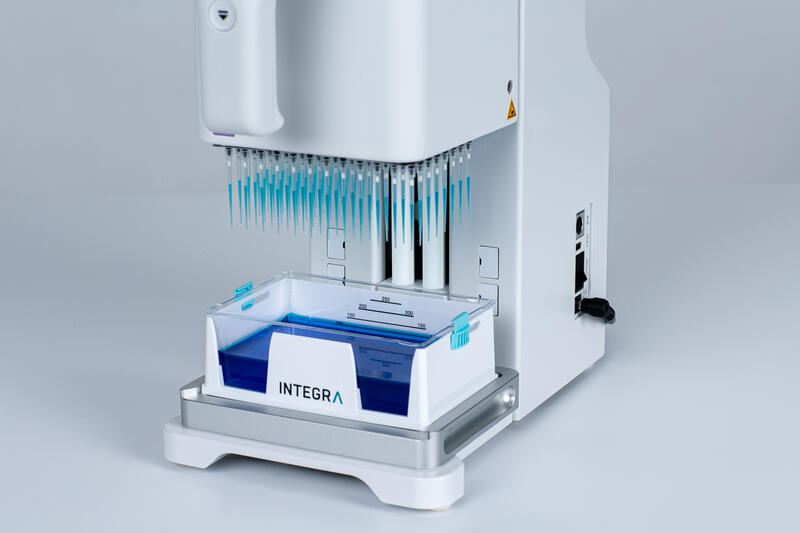
シーケンスベースのアプローチの適用
耐性マーカー遺伝子の中には、塩基配列のばらつきが大きいためqPCR解析では特定できないものもあります。したがって、古典的なサンガーシーケンシング解析によってさらに配列決定できるよう、qPCR産物を精製しなければなりません。INTEGRAのソリューションのラインアップは、この可能性に容易に対応することができます。例えば、VIAFLO 96電動プレート分注機を使用すると、この追加の精製ステップをスピードアップさせることができ、結果の信頼性を高めつつ、時間を大幅に節約することができます。しかし、サンガーシーケンシングは一度に1つの耐性遺伝子しか標的にできない、別のシーケンシングベースの方法である次世代シーケンシング(NGS)が近年広がりつつあります。

NGSでは、より高いスループットが得られ、アンプリコン特異的法(より速い)、またはディープシーケンシングと呼ばれる全ゲノム法のいずれかが利用されます。NGSは非常に高感度で、使用液量が非常に少ないため、正確な分注が極めて重要です。しかし、分注手順が長いとスタッフは疲労や不快感を感じてしまう場合があるため、現代の研究室では液体処理ステップの広範な自動化が必要になります。シーケンシングに関連する面倒な作業(– プーリングや陽性サンプルヒットピッキングなど) の多くは、ASSIST PLUS分注ロボットおよびD-ONEシングルチャンネル分注モジュールを使用して完全に自動化でき、研究室の生産性と結果の再現性を向上させることが可能です。同じセットアップを使用して、DNAライブラリーのノーマライゼーションを容易に行うこともできます。これらの革新的な人間工学に基づく製品は、人為的エラー、身体的負担、有害な微生物への曝露リスクを最小限に抑えることにも役立ち、これらは間違いなくASTにおける最優先事項です。

MDR菌に打ち勝つために
新しい抗生物質は開発に長い期間を要するため、臨床医は現在利用可能な抗生物質を慎重に使用しなければなりません。MDR病原体を迅速に検出することは、できる限り早く患者を正しい治療経路に導くのに役立ち、患者の回復を早め、転帰が良好となる可能性を高めることにつながります。堅牢で高品質なピペットプラットフォームによる自動化は、抗微生物薬耐性の迅速な特定における重要な側面であり、INTEGRAの革新的な製品ラインアップは、この継続する戦いにおいて価値のある投資となります。